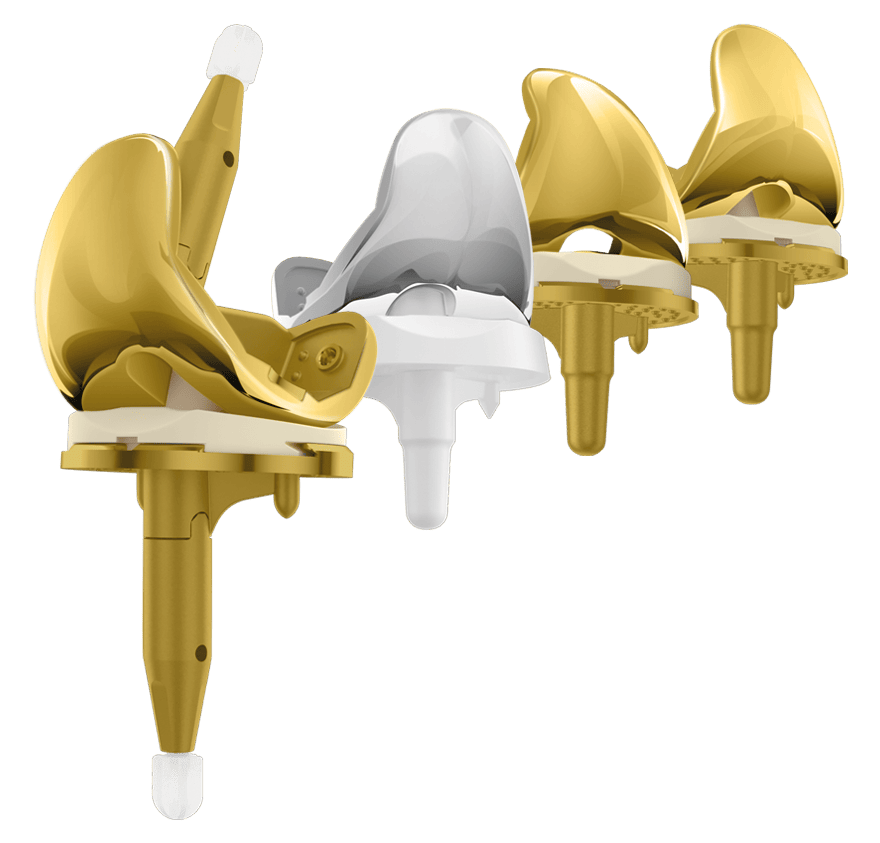
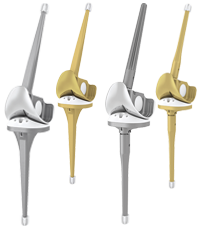
Die dynamischen TrabecuLink Femur- und Tibiakonen sind eine attraktive Lösung für die zementfreie Rekonstruktion von Knochendefekten10 sowie zur zusätzlichen Unterstützung der Prothese bei Knochenverlust in der proximalen Tibia. Die Kombination aus dynamischer Ausführung5, 6 der Konen und dem biokompatiblen Material Tilastan-E11,12 bietet die ideale Voraussetzung für eine stabile und dauerhafte Verankerung und eine erfolgreiche Knochenregeneration.
Die dreidimensionale TrabecuLink Struktur bietet aufgrund ihrer Porengröße, Porosität und Strukturtiefe eine hervorragende Grundlage für die Förderung der Osteokonduktion und Mikrovaskularisation. Dabei werden die Anforderungen an die strukturdeckende Proteinschicht (Fibronectin, Vitronectin, Fibrinogen) berücksichtigt.1,2 Die TrabecuLink Konen sind mit der bewährten LINK Endo-Modell Kniefamilie und LinkSymhoKnee CCK kombinierbar, die in zahlreichen Größen und Varianten erhältlich ist. Das Größenangebot entspricht den Dimensionen der achsgeführten
Knieendoprothesen.
Stabil in der metaphysären Verankerung9,13
- Verstärkung der Knochenstruktur bei femoralen und tibialen Knochendefekten
- Hohe Primärstabilität für den TrabecuLink Konus sowie für die darin einzementierte Gelenkkomponente
- Knochenseitig zementfrei zur Knochenregeneration
Schützend durch innere Metallwand
- Verhindert das Eindringen von Knochenzement in die TrabecuLink Struktur
- Zuverlässige Zementfixierung durch speziell positionierte „Nuten“ (revisionsfreundlich)
Elastisch durch integrierte Biegeachsen in der inneren Metallwand
- Mechanische Kompression zur Förderung der Knochenregeneration5,6
- Biegeachsen für eine individuelle Anpassung
- Gute Passform und vereinfachtes Einsetzen der TrabecuLink Femur-/Tibiakonen durch strukturelle Elastizität
- Federeffekt zur Vereinfachung der intraoperativen Positionierung
Umweltschonend3,8
- Ressourcenschonende Herstellung aus bewährter Titanlegierung
Vielseitig – für zahlreiche Anwendungsfälle7
- Kombinierbar mit allen Femur- und Tibiakomponenten der LINK Endo-Modell Kniefamilie
- Größen entsprechend den Dimensionen der achsgeführten Knieendoprothesen
- Patientenspezifische Sondermodelle auf Anfrage herstellbar
TrabecuLink
dreidimensionale Struktur für eine optimale Knochenanlagerung
- Die Porengeometrie (Porosität: 70 %, Porengröße: 610–820 μm, Strukturtiefe: bis zu 2 mm) gewährleistet eine hervorragende Zellanlagerung.1,2,4
Porenfüllung
Die Bildfolge zeigt das Füllen einer Pore der TrabecuLink Struktur mit Gewebe in einer In-vitro-Zellkultur. Als grüne Fasern zu erkennen ist das von humanen Fibroblasten über einen Zeitraum von acht Tagen abgelegte und kontinuierlich reorganisierte Fibronektin. Fibronektin ist eine früh im Heilungsprozess gebildete Komponente der extrazellulären Matrix. Es stellt eine Vorlage für die Einlagerung von Kollagen dar, welches wiederum essentiell für die Mineralisierung des Gewebes und das Einwachsen von Knochen in die Struktur ist. Neben der mit der Zeit zunehmenden Menge an Fibronektin ist eine deutliche Kontraktion der Matrix in Richtung des Zentrums der Pore zu beobachten. Dieser auf den im Gewebe wirkenden Zellkräften beruhende Kontraktionsmechanismus beschleunigt das Auffüllen der Pore mit Gewebe im Vergleich zu einem Schicht-auf-Schicht-Gewebewachstum (Referenz: Joly P et al., PLOS One 2013; https://journals.plos.org/plosone/article?id=10.1371/journal.pone.0073545). Julius Wolff Institut, Charité – Universitätsmedizin Berlin
Quelle
- Cecile M. Bidan, Krishna P. Kommareddy, Monika Rumpler, Philip Kollmannsberger, Yves J.M. Brechet, Peter Fratzl, John W.C. Dunlop. et al.; How Linear Tension Converts to Curvature: Geometric Control of Bone Tissue Growth; PLoS ONE 7(5): e36336. https://doi.org/10.1371/journal.pone.0036336 (2012)
- Pascal Joly, Georg N. Duda, Martin Schöne, Petra B. Welzel, Uwe Freudenberg, Carsten Werner, Ansgar Petersen, et al.; Geometry-Driven Cell Organization Determines Tissue Growth in Scaffold Pores: Consequences for Fibronectin Organization; PLoS ONE 8(9): e73545. doi.org/10.1371/journal.pone.0073545 (2013)
- Dr. Malte Drobe, Franziska Killiches; Vorkommen und Produktion mineralischer Rohstoffe – ein Ländervergleich; Bundesanstalt für Geowissenschaften und Rohstoffe Hannover; http://www.bgr.bund.de/DE/Themen/Min_rohstoffe/Downloads/studie_rohstoffwirtschaftliche_einordnung_2014.pdf?__blob=publicationFile&v=4 (2014)
- Steinemann SG; Compatibility of Titanium in Soft and Hard Tissue – The Ultimate is Osseointegration; Materials for Medical Engineering, WILEY-VCH, Volume 2, Page 199-203
- Gerald Küntscher; Praxis der Marknagelung; Friedrich-Karl Schattauer-Verlag (1962)
- R. Texhammer, C. Colton et al.; AO-Instrumente und Implantate (Technisches Handbuch); Springer Verlag, 2. Auflage, S.25 (2011)
- Gabriele Panegrossi, corresponding author Marco Ceretti, Matteo Papalia, Filippo Casella, Fabio Favetti, and Francesco Falez; Bone Loss Management in Total Knee Revision Surgery; Int Orthop. 2014 Feb; 38(2): 419–427; www.ncbi.nlm.nih.gov/pmc/articles/PMC3923937/ (2014)
- Conflict Minerals: MEPs Secure Mandatory Due Diligence for Importers; Press release - External/international trade − 22-11-2016 - 19:07; www.europarl.europa.eu/news/en/news-room/20161122IPR52536/conflict-minerals-meps-secure-mandatory-due-diligence-for-importers (2016)
- Henricson A, Linder L, Nilsson KG.; A Trabecular Metal Tibial Component in Total Knee Replacement in Patients Younger than 60 Years: a Two-year Radiostereophotogrammetric Analysis; J Bone Joint Surg Br. 2008;90:1585–1593. doi: 10.1302/0301-620X.90B12.20797 (2008)
- P. K . Sculco, M. P. Abdel, A. D. Hanssen, D. G. Lewallen; The Management of Bone Loss in Revision Total Knee Arthroplasty; Bone Joint J 2016;98-B(1 Suppl A):120–4 (2016)
- Peter Heinl, Lenka Müller, Carolin Körnera, Robert F. Singera, Frank A. Müllerb; Cellular Ti–6Al–4V Structures with interconnected Macro Porosity for Bone Implants Fabricated by Selective Electron Beam Melting; Acta Biomaterialia Volume 4, Issue 5, September 2008, Pages 1536–1544 (2008)
- Hong Wang, Bingjing Zhao, Changkui Liu, Chao Wang, Xinying Tan, Min Hu; A Comparison of Biocompatibility of a Titanium Alloy Fabricated by Electron Beam; PLOS ONE | DOI:10.1371/journal.pone.0158513 July 8 2016, (2016)
- Ivan De Martino, Vincenzo De Santis, Peter K Sculco, Rocco D’Apolito, Joseph B Assini, Giorgio Gasparini; Tantalum Cones Provide Durable Mid-Term Fixation in Revision TKA; Clin Orthop Relat Res 473 (10), 3176-3182 (2015)